分子の鋳型を取る分子インプリンティング技術Molecular Imprinting technology
私たちは30年以上も分子の鋳型を取る分子インプリンティングに関する研究を行っている日本で唯一の研究室です。この技術で生み出される材料「分子鋳型」は、分子インプリントポリマー(Molecularly Imprinted Polymers)と呼ばれ、MIPsと略されます。
例えば石膏で型を取った右手のギブスは、左手にはフィットしないように、特定の分子に対するMIPsは、その分子を他の分子と見分けて結合することができます。すなわち、MIPsは、特定分子を選択的に「分子認識」して結合できる人工高分子材料です。
MIPsは、私たちの体の中にある「抗体」と同様の機能をもちます。その上、安価で安定に大量生産できることから、高価で不安定な抗体などの生物由来の材料に替わる材料として、分離分析素材やセンサー素材をはじめ、薬物送達システムやナノメディシンなどに広く応用され、大きな注目を集めています。
We are the only research laboratory in Japan that has conducted over 30 years of dedicated research on molecular imprinting, a technique used to create “molecular templates.” The materials developed using this technology are called Molecularly Imprinted Polymers, commonly known as MIPs.
Just like a plaster cast made from your right hand won’t fit your left, MIPs are tailor-made to recognize and bind only to a specific molecule. These advanced synthetic materials are capable of molecular recognition, enabling them to selectively identify and capture their target—just like a lock that fits only one key.
MIPs function much like the antibodies found in our bodies—they can selectively recognize and bind to specific target molecules. However, unlike biological antibodies, MIPs can be produced inexpensively, in large quantities, and with excellent stability. Thanks to these advantages, MIPs are gaining widespread attention as next-generation alternatives to biological materials. Their applications range from separation and analytical materials to sensors, drug delivery systems, and cutting-edge nanomedicine.
分子の鋳型を取るー 第一世代分子インプリンティング
基本的に、認識したい分子(鋳型分子と呼ぶ)を共存させた状態で高分子を合成し、その後、高分子から鋳型分子を取り除くとこで、鋳型分子の形状を記憶した空孔が形成されます。
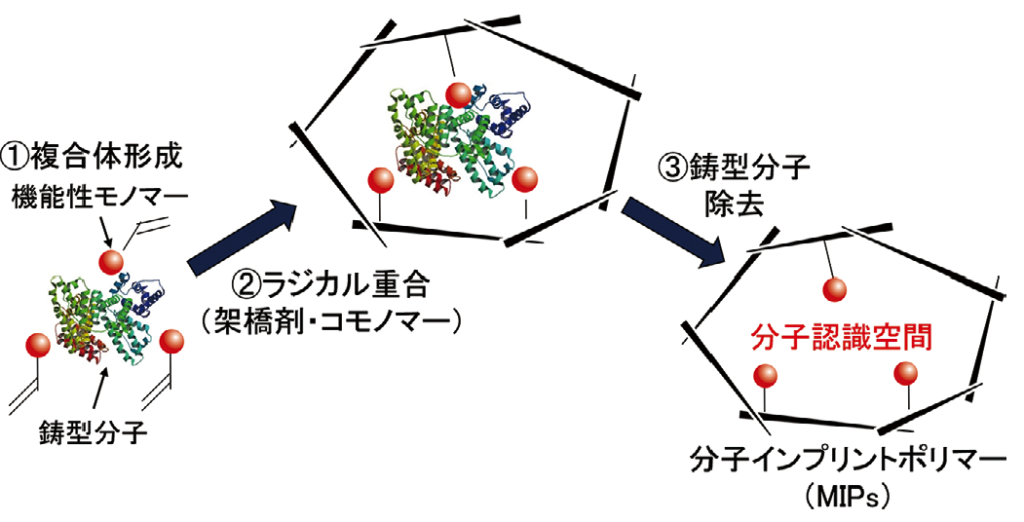
分子インプリンティングの概念図
上図のように、①「鋳型分子」および「鋳型分子と結合する官能基をもつモノマー(機能性モノマー)」で「複合体」を形成させた後、② 架橋剤や他のモノマーを含む重合溶液中に添加して重合します。③ 重合後、複合体の周りに高分子材料が形成されるため、鋳型分子を除去した後に高分子内に残される空孔は、 鋳型分子の形状が記憶されると同時に、機能性モノマー由来の官能基が、鋳型分子と相互作用するのに都合のいい位置に配置されます (分子認識空間の形成)。これにより、MIPsは、鋳型分子に対し、高い選択性と親和性を発現します。
MIPsは、鋳型分子に合わせてデザインできることから、原理的に非常に広範な分子に対する認識材料を創製できます。また、鋳型分子周辺に形成される高分子材料の形状を制御することで、薄膜状や粒子状などのさまざまな形状でMIPsを合成できます。
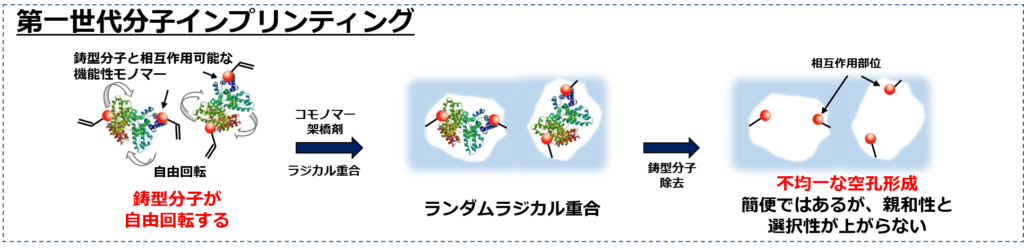
第二世代分子インプリンティング
低分子MIPsーコルチゾール
例えば、ストレスの指標として注目されているステロイド骨格をもつ低分子化合物の「コルチゾール」に対するMIPsは以下のように合成されます。鋳型分子は、片側には、アダマンタンを導入した。理由は、アダマンタンと強い相互作用をするβ-シクロデキストリンを固定化した基板上に、鋳型分子を同じ方向で固定化するためである。この配向固定化は、空孔の均一性を上げるのに役立つ。また、基板上に残るβ-シクロデキストリンは、コルチゾールとも相互作用があるので、鋳型分子の配向固定化とコルチゾールの結合部位との両方の役槍を担う。
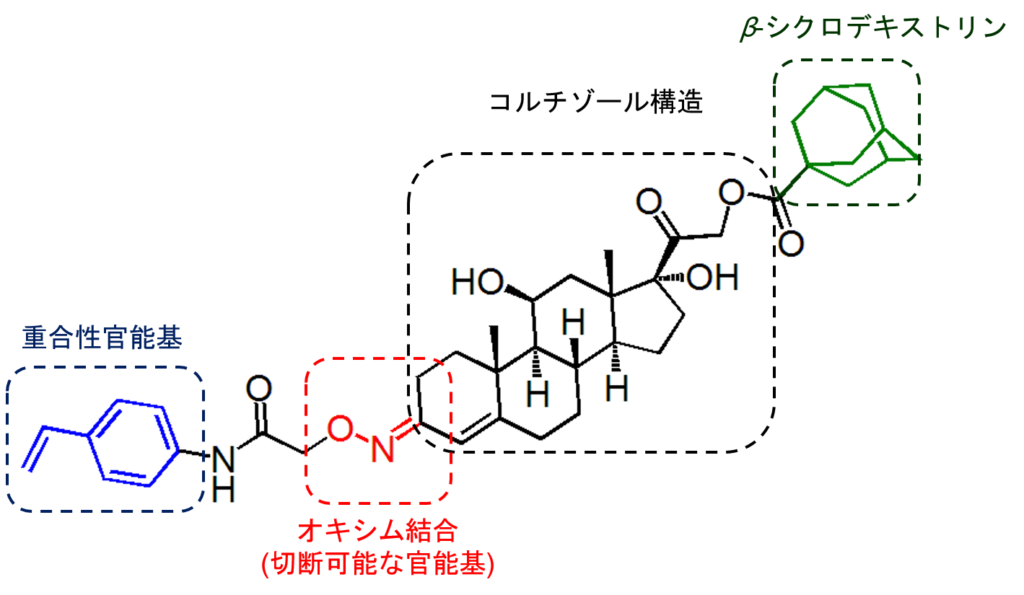
コルチゾールMIPs合成のために設計された鋳型分子
もう片側には、重合可能な官能基をもつモノマーを切断可能なオキシム結合で連結した。架橋剤と子モノマーを添加して、表面開始原子移動ラジカル重合を行い、薄膜を形成した後、オキシム結合を加水分解して鋳型分子を取り出すと、奥に β-シクロデキストリン、上方にアミノ基が配置されたコルチゾール結合空孔が形成された。ここでは、コルチゾールは、3位のカルボニル基が空孔内アミノ基と、ステロイド骨格のD環は 空孔底部の β-シクロデキストリンと2点での相互作用をすることになる。
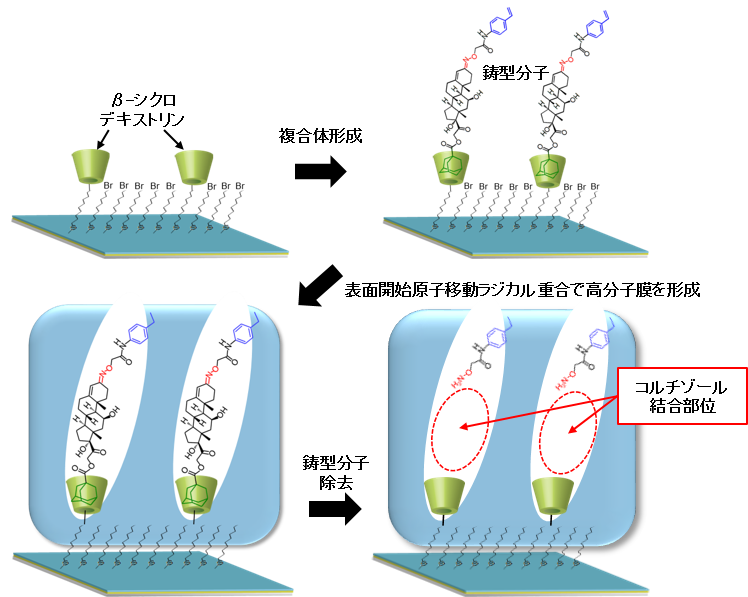
コルチゾールMIPsの合成手順
実際、このMIP薄膜を用いて蛍光競合法にてコルチゾールを測定したところ、検出限界は約8 pMと算出され、唾液中のコルチゾールが測定可能なぼどの高感度検出を達成した。また、コルチゾールの構造類似体である17β-エストラジオール, コレステロール, テストステロン, プロゲステロンに対する応答は、コルチゾールよりも明らかに低く、MIP薄膜は、高感度、高選択的にコルチゾールを認識していることが示された。
タンパク質MIPsー
MIPナノ粒子による薬物送達システム
To be Beyond Natural Antibodies-天然の抗体を超える戦略
タンパク質は、遺伝情報を翻訳して生合成されます。ただし、多くのタンパク質は、生合成後、さらに化学的な修飾を受けて機能化されます。この過程は、タンパク質の「翻訳後修飾 (Post-translational modification)」として知られています。
このタンパク質の機能化戦略「翻訳後修飾」を、MIPsに適用したらどうだろう? 天然の抗体を超える機能をもった人工材料が創成できる?
ポストインプリンティング修飾による高機能化戦略
「翻訳後修飾」と同様に、分子の鋳型を取った後、さらに機能性分子で化学修飾するポストインプリンティング修飾(Post-imprinting modification)を行うことで、結合特性の調整、結合情報の可視化、分子認識能のスイッチングなど、従来の分子インプリンティングでは不可能だった高機能化・多機能化が達成できることお世界で初めて達成しました。分子認識対象は多岐にわたり、抗生物質や環境ホルモンからタンパク質、細胞外小胞エクソソーム、細胞にいたる様々な物質に適用可能でした。